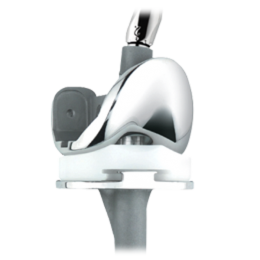
Ürün Açıklaması
NexGen RH Diz tibia kondil, tarafından yürütülmektedir yükün% 95 ile sonuçlanan bir modüler menteşe mekanizması sunar1 primer implant tasarımı yükleme desenine benzer.
Condylus hareket aralığı boyunca kaval kemiği üzerinde merkezlenmiş olarak kalır ve patella oluk şeklindeki bir tasarımı ile benzer olduğu için NexGen sistem, patella takip bir primer tasarlamak için diz benzer.
Daha zorlu artroplastisi prosedürleri için, NexGen RH Diz ile birlikte kullanılabilir Trabeküler Metal ™ Tibial ve Femoral Konileri * adresi bu en zor kemik kaybı senaryoları.
Yana NexGen RH Diz kullanılarak modüler tasarım yararlanır NexGen artırmaktadır, temel kemik kesimler için yapılanlar aynıdır NexGen İlköğretim Sistem Bileşenleri. Bu kemik kaybını en aza indirmek için yardımcı olur ve sık primer implant işlemlerinde kullanılan enstrümanların kullanımı sağlar.
Ile birlikte kullanıldığında * kemik çimentosu ile kullanılması gerekir NexGen RH Diz.
Patellofemoral femoral Kinematiği
NexGen RH Diz Femoral Bileşen diğer aynı patello-femoral tasarıma sahiptir NexGen Femoral Bileşenleri. Anatomik patella benzer – oluk patellanın derinden izlemenize olanak sağlar. Patella tam fleksiyon 60 ° ‘ye kadar desteklenir. Menteşe ekseni, merkezi bir konumda bir tutarlı sagital düzlem içinde condylus tutar. Patella fleksiyon sırasında vitreus kaymamasını Bu daha başlangıç, normal patella izleme sağlar.
Etki sınırlamak için tasarlanan, Subluksasyonu Resist
Subluksasyon direnmek için, NexGen RH Diz kilitleme mekanizması tasarımı 40 mm’lik minimum bir “sıçrama yüksekliği” sunuyor.
Femoral kondil ve yüksek bombeli tibial eklem yüzeyi arasındaki uygunluk oranı neredeyse 1 ile 1 olduğunu. Temas alanı maksimize ederek, polietilen stresler daha geniş bir alana dağılmış olan.
İletişim ve frontal yarıçapı oluşur NexGen implant hiperekstansiyon hareket gibi artiküler yüzeyi ile RH Diz Femoral Komponent. Bu diz uzatma etkisi nemlendirme, biraz rahatsız etmek için neden olacaktır. Bu etkileşim hiperekstansiyon gücü dağıtmak için tasarlanmıştır.
Pivot / Dönme
Merkezi konumu NexGen RH Diz menteşe mekanizması menteşe diz tasarımları posteriora göre daha doğal ve tutarlı tibio-femoral kinematiği sonuçlanan yakın tibial komponent eksenine yerleştirilir. Dönme NexGen RH Diz platformu iç ve dış rotasyon hareketinin 25 dereceye kadar izin verir bu yana, yumuşak dokulara çimento arabirimleri burulma displace için tasarlanmıştır.
Menteşe Pim / Kilitleme Mekanizması Modülerlik
Menteşe piminin sonrası uzantı modülerliği implantasyon parçaları monte edilirken diz aşırı deli ya da tutulması gerekmeksizin yürümesine imkan verir. NexGen RH Diz Femoral ve Tibial Bileşenler konuma yapıştırılır ve minimal distraksiyon ile tibia eklem yüzeyinin pozisyona döndürülür vardır. Menteşe sonrası uzantısı kolayca tibia taban plakası yerleştirilir ve sıkılır.
95% Condylan Yükleniyor
Tam uzantı elde edilene kadar bir çok geleneksel döner mafsal diz tasarımlarda, menteşe sıkışma yükünün büyük taşımaktadır. Posteriora yer dönme merkezine sahip Tasarımlar çimento arabirimleri veya menteşe hızlandırılmış polietilen taşıyan aşınma üzerinde stres neden olabilir ortak “rezervasyon”, neden olabilir. NexGen RH Diz RH Diz femoral komponent ve eklem ROM boyunca merkezi iletişim (hiperekstansiyon -3 ° den 120 ° ‘ye) korumak için tasarlanmıştır olarak bu endişeleri giderir. Patentli menteşe tasarım özellikleri tibia kondil ile yükün% 95’i geçmektedir.
Temizleme Talimatları
Sterilite
Gama ışınlaması etiketleme sembolü ile gösterilir. Ambalaj bütünlüğü ihlal edilmemiştir gibi bu cihazlar sürece steril kalır.Kullanmadan önce her paket kontrol edin ve herhangi bir mühür veya kavite hasarlı veya ihlal veya son kullanma tarihi aşıldığında ise bileşen kullanmayın. Açıldıktan sonra bileşen kullanılması gerekir, atılır, ya da tekrar sterilize.
Tekrar Sterilizasyon Talimatları
Bunlar sterilizasyon talimatları ANSI / AAMI / ISO standartları ve ilkeleri ile uyumludur. Onlar yeniden işleme yeniden cihazlar için, veya açılmış ancak kullanılmayan edildi ve steril ürün için, steril ürünler için kullanılmalıdır. Tekrar kullanılabilen aletler ve provisionals için ayrıntılı sterilizasyon kılavuzlar için Zimmer kitapçık 97-5000-170-00 (distribütörünüzle edinilebilir) bakın.
Katı metal implantlar cerrahi için hazırlanırken sterilite yanlışlıkla kaybı durumunda, acil kullanım için sadece bir kez tekrar sterilize edilebilir. Bu aşağıda listelenen istisnalara tabidir.
Tekrar sterilize etmeyin
- Vücut sıvıları veya enkaz ile kirlenmiş veya oylandı Tek kullanımlık-Sadece bileşenler önceden implante edilmiştir
- Trabeküler Metal ™ Teknolojisi bileşenleri
- UHMWPE içeren Bileşenleri
- PMMA içeren Bileşenleri
Yeniden sterilizasyon için orijinal plastik boşluklar veya kapaklar kullanmayın. Tek cihazlar standart bir polietilen veya Tyvek kullanabilirsiniz ® poşet. Kese mühürler vurgulayarak veya kese yırtmadan cihazlar içerebilecek kadar büyük olduğundan emin olun.
Plastikten yapılmış herhangi bir sterilizasyon olguların üstüne ağır eşyalar koymayın. Elde edilen deformasyon plastik malzemenin çatlamaya neden olabilir.
Tiftiği veya enkaz (USP arıtılmış su kullanan) kaldırmak için gözenekli durulayın.
Deterjan ve fırça ile Agresif temizlik elyaf metal balatalı veya boncuk kaplama olarak implantın özellikleri, zarar verebilir.Ayrıca, bazı deterjanlar özellikle polimer ürün, silikon kauçuk yapılanlar durulayın zor olabilir.
Titanyum ve titanyum alaşımları yapılmış ürünler buhar kazanı arıtma kimyasalları veya deterjan artıkları oksit katmanları oluşturabilir. Bu oksitler biyouyumlu olmakla birlikte, gravürler ve stampings yoketmek.
Modüler implant bileşenler ölü boşluk ve genişleme / daralma gerilmeler olası biyolojik yük birikimini en aza indirmek için ayrı ayrı sterilize edilmelidir.
Ürün Broşürü
Indications
Individualization of Treatment
Contraindications
- This product for other than labeled indications (off-label use)
- Any component if damage is found or caused during setup or insertion
- Components from other knee systems (and vice versa) unless expressly labeled for such use. Premature wear or loosening may develop and may require surgical explantation
- Micro-sized patellas with the Rotating Hinge Knee. Excessive wear may result
- 26 or 29 mm-sized standard patellas with B, C, D, E, or F femoral components unless used in an inset mode. Excessive wear may result
- Avoid notching, scratching, or striking the device
- The potential for deep sepsis can be minimized by using biocontamination controls. Continued surveillance for new or recurrent sources of infection should be continued as long as the device is in place.
- Loosening or fracture/damage of the prosthetic knee components or surrounding tissues
- Dislocation and/or joint instability
- Malalignment of the prosthetic knee components
- Bone fracture or nerve damage
- Swelling or infection
- Leg length discrepancies
- Poor range of motion
- Pain
- Venous thromboembolic disease
- Inflammation
- Metal sensitivity
- Corrosion of metal components (the significance and long-term implications are uncertain and await further clinical evidence and evaluation)